Hòa tan hoàn toàn 1,35 gam oxit kim loại M hóa trị III vào dung dịch axit HCL thu được 1,68 lít khí H2 (đktc). Hãy xác định kim loại M?

Những câu hỏi liên quan
Hòa tan hoàn toàn 5,6 gam một kim loại X hóa trị II vào dung dịch axit clohiđric HCl, thu được 2,24 lít khí H2 (đktc). Xác định kim loại X:
A. Mg
B. Fe
C. Zn
D. Cu
Số mol của khí hidro ở dktc
nH2 =\(\dfrac{V_{H2}}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : X + 2HCl → XCl2 + H2\(|\)
1 2 1 1
0,1 0,1
Số mol của kim loại X
nX = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ MX = \(\dfrac{m_X}{n_X}=\dfrac{5,6}{0,1}=56\) (dvc)
Vậy kim loại x là Fe
⇒ Chọn câu : B Chúc bạn học tốt
Đúng 2
Bình luận (0)
\(R+2HCl \rightarrow RCl_2+H_2\\ n_{H_2}=\frac{2,24}{22,4}=0,1mol\\ M_R=\frac{5,6}{0,1}=56 g/mol\\ \Rightarrow R: Fe\)
Đúng 0
Bình luận (0)
bài 1:cho 7,2g kim loại hóa trị II phản ứng hoàn toàn 100ml dung dịch HCL 6M. Xác định tên kim loại đã dùng
baì 2: hòa tan hoàn toàn 7,56g kim loại R có hóa trị III vào dung dịch axit HCL thu được 9,408 lít H2 (đktc). Tìm kim loại R
Giúp mik vs ạ ! Cảm ơn
Bài 1:
Gọi KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Ta có: \(n_{HCl}=0,1.6=0,6\left(mol\right)\)
Theo PT: \(n_A=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{7,2}{0,3}=24\left(g/mol\right)\)
Vậy: KL cần tìm là Mg.
Đúng 1
Bình luận (0)
Bài 2:
PT: \(2R+6HCl\rightarrow2RCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{9,408}{22,4}=0,42\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{3}n_{H_2}=0,28\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{7,56}{0,28}=27\left(g/mol\right)\)
Vậy: R là Al.
Đúng 1
Bình luận (0)
Bài 24. Hòa tan 3,6g một kim loại A hóa trị II bằng một lượng dư axit HCl thu được 3,36 lít khí H2 (đktc). Xác định tên kim loại ABài 25. Hòa tan hoàn toàn 8,1g kim loại A hóa trị III trong dd HCl dư thu đucợ 10,08 lít khí H2 (đktc). Xác định tên A và m HCl đã dùng
Đọc tiếp
Bài 24. Hòa tan 3,6g một kim loại A hóa trị II bằng một lượng dư axit HCl thu được 3,36 lít khí H2 (đktc). Xác định tên kim loại A
Bài 25. Hòa tan hoàn toàn 8,1g kim loại A hóa trị III trong dd HCl dư thu đucợ 10,08 lít khí H2 (đktc). Xác định tên A và m HCl đã dùng
Bài 24:
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ PTHH:A+2HCl\rightarrow ACl_2+H_2\uparrow\)
Theo pthh: nA = nH2 = 0,15 (mol)
=> MA = \(\dfrac{3,6}{0,15}=24\left(\dfrac{g}{mol}\right)\)
=> A là Mg
Bài 25:
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\\ PTHH:2A+6HCl\rightarrow2ACl_3+3H_2\uparrow\\ Mol:0,3\leftarrow0,9\leftarrow0,3\leftarrow0,45\\ \rightarrow\left\{{}\begin{matrix}M_A=\dfrac{8,1}{0,3}=27\left(\dfrac{g}{mol}\right)\Rightarrow A:Al\\m_{HCl}=0,9.36,5=32,85\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (1)
Bài 24.
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(n_A=\dfrac{3,6}{M_A}\) mol
\(A+2HCl\rightarrow ACl_2+H_2\)
0,15 0,15 ( mol )
\(\Rightarrow\dfrac{3,6}{M_A}=0,15mol\)
\(\Leftrightarrow M_A=24\) ( g/mol )
=> A là Magie ( Mg )
Bài 25.
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45mol\)
\(n_A=\dfrac{8,1}{M_A}\) mol
\(2A+6HCl\rightarrow2ACl_3+3H_2\)
0,3 0,45 ( mol )
\(\Rightarrow\dfrac{8,1}{M_A}=0,3\)
\(\Leftrightarrow M_A=27\) g/mol
=> A là nhôm ( Al )
Đúng 1
Bình luận (0)
. Hòa tan hoàn toàn 16,25 gam kim loại M (chưa rõ hóa trị) vào dung dịch axit HCl dư. Khi phản ứng kết thúc thu được 5,6 lít H2 (đktc).
a. Xác định kim loại M trong số các kim loại cho sau: Na=23; Cu=64; Zn=65.
b. Tính thể tích dung dịch HCl 0,2M cần dùng để hòa tan hết lượng kim loại này.
a) \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
\(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,5}{n}\left(mol\right)\)
Ta có : \(M_M=\dfrac{16,25}{\dfrac{0,5}{n}}=32,5n\)
Chạy nghiệm n
n=1 => M=32,5 (loại)
n=2 => M=65 ( chọn)
n=3 => M=97,5 (loại)
Vậy M là Zn
b) Ta có : \(n_{HCl}=2n_{H_2}=0,5\left(mol\right)\)
=> \(V_{HCl}=\dfrac{0,5}{0,2}=2,5\left(lít\right)\)
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 4 gam hỗn hợp gồm Fe và một kim loại hóa trị II vào dung dịch HCl dư, thu được 2,24 lít khí H2 (đktc). Nếu chỉ dùng 2,4 gam kim loại hóa trị II thì sử dụng không hết 0,5 mol HCl. Xác định tên kim loại hóa trị II.
1.Dùng H2 khử 16gam oxit kim loại hóa trị III, thu được 11,2gam kim loại A. Xác định A
2.Cho 8,1 gam kim loại M tác dụng với dung dịch HCL dư thu được 10,08 lít H2 ở đktc. Xác định kim loại M biết M hóa trị III
Câu 1:
A2O3 + 3H2 -t0-> 2A + 3H2O
2A+48...................2A
16..........................11.2
<=> 11.2 * (2A + 48) = 16 * 2A
=> A = 56
Vậy A là : Fe
Đúng 2
Bình luận (1)
nH2 = 10.08/22.4 = 0.45 (mol)
2M + 6HCl => 2MCl3 + 3H2
0.9...............................0.45
MM = 8.1/0.3 = 27
M là : Al
Đúng 1
Bình luận (0)
1.
3H2+A2O3----t°--}2A+3H2O
Gọi nH2=nH2O=a mol
Áp dụng định luật bảo toàn khối lượng,ta có
2a+16=11,2+18a
16a=4,8
a=0,3(mol)
Theo pt:
nA=2/3.nH2=2/3.0.3=0,2(mol)
MA=11,2/0,2=56(g/mol)
A Là Zn
Đúng 0
Bình luận (1)
Xem thêm câu trả lời
Khử 4,8 gam một oxit của kim loại trong dãy điện hóa ở nhiệt độ cao cần 2,016 lít khí H2 đktc . Kim loại thu được đem hòa tan trong dung dịch HCl thu được 1,344 lít khí H2 đktc . Hãy xác định công thức hóa học của oxit đã dùng: A. Fe2O3 B. MgO C. Fe3O4 D. Al2O3
Đọc tiếp
Khử 4,8 gam một oxit của kim loại trong dãy điện hóa ở nhiệt độ cao cần 2,016 lít khí H2 đktc . Kim loại thu được đem hòa tan trong dung dịch HCl thu được 1,344 lít khí H2 đktc . Hãy xác định công thức hóa học của oxit đã dùng:
A. Fe2O3
B. MgO
C. Fe3O4
D. Al2O3
Đáp án A
Oxit chưa biết của kim loại nào → Gọi MxOy
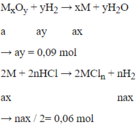
Mà : 56ax + 16ay = 4,8
→ ax = 0,06
→ x : y = ax : ay = 0,06 : 0,09 = 2 : 3 => M2O3
→ n = 0,12 : 0,06 = 2 => M hóa trị II
→ Chỉ có Fe thỏa mãn vì nó có hai hóa trị
Lưu ý: Bài toán này dễ nhầm lẫn nếu không để ý sự thay đổi hóa trị ở 2 phương trình.
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 6,5 gam một kim loại A chưa rõ hóa trị vào dung dịch HCl thì thu được 2,24 lít khí hidro(đktc) . Xác định kim loại A
Gọi hóa trị của kim loại A là x
\(n_{H_2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH : 2A + 2xHCl -----> 2AClx + xH2
0,2/x mol 0,1mol
Áp dụng m = n.M , ta có : \(A.\frac{0,2}{x}=6,5\Rightarrow A=32,5x\)
Do x là hóa trị của kim loại nên x chỉ có thể là I , II hoặc III
Nếu x = 1 thì A = 32,5 (loại)
Nếu x = 2 thì A = 65 (nhận)
Nếu x = 3 thì A = 97,5 (loại)
Vậy A là kim loại Kẽm (Zn)
Đúng 2
Bình luận (2)
nH2= 0,1 (mol)
2A + 2nHCl -> 2ACln + nH2
Theo PTHH
=> \(\frac{6,5}{A}=\frac{2}{n}\cdot0,1\)
=> 6,5n = 0,2A
=> 32,5n =A
Với A là kim loại tác dụng được vs HCl => hóa trị chỉ có thể từ 1 tới 3
Thay vào ...
=> n= 2
A = 65
=> A là Zn
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 9,2 gam kim loại kiềm M vào nước thu được dung dịch A và 4,48 lít khí H2 (đktc) Xác định tên kim loại
Xem chi tiết
\(2M+2H_2O\rightarrow2MOH+H_2\)
0,4 mol \(\leftarrow\) 0,2 mol
Khối lượng mol của \(M\) là:
\(M=\dfrac{m}{n}=\dfrac{9,2}{0,4}=23\)
Vậy \(M\) là kim loại \(Na\)
Đúng 2
Bình luận (0)
































